
CAR-T细胞疗法因临床疗效显著成为了肿瘤治疗领域的研究热点,并被《科学》列为十大科学突破之首。近年随着技术的进步,细胞治疗涌现出了更多疗法,治疗领域也从血液瘤扩展到了实体瘤治疗,技术手段从单一免疫细胞发展到了合成免疫细胞组库。CAR-T疗法和合成免疫疗法目前研究现状如何?面临哪些挑战?
12月23日,上海市药物研发协同创新中心与浦东国际人才发展中心共同举办第45期 science café活动。本期特别邀请科济药业控股有限公司早期研发副总裁、原上海市肿瘤研究所蒋华教授和海军军医大学基础医学院胡适教授,为大家分享细胞治疗研究现状、面临的挑战以及应对策略。
以下是嘉宾报告精彩内容:
1、CAR-T治疗实体瘤面临的挑战及应对策略
蒋华教授从CAR-T细胞治疗的研究现状及其优势出发,介绍并剖析了CAR-T治疗实体瘤面临的挑战和策略。
CAR-T细胞疗法近年一直是肿瘤免疫治疗的研究热点,也是先进技术之一,它整合了细胞技术、免疫技术以及基因工程技术。在2013年,以CAR-T为代表的肿瘤免疫治疗被《科学》杂志列为十大科学突破之首。自此,CAR-T发展进入了快车道,随着临床试验的成功,CAR-T细胞治疗也被认为是最有希望治愈肿瘤的疗法之一。
CAR-T细胞临床治疗流程分为5个步骤,具体为:从患者体内外周血提取淋巴T细胞,将T细胞体外活化,随后通过基因重组的方法将CAR基因转入T细胞,经体外大量扩增,最后再回输患者体内。蒋教授介绍到,与传统药物治疗相比,CAR-T细胞治疗有三大优势:第一具有卓越的治疗潜力,它可以克服传统药物的耐药或复发;第二具有独特的治疗方式,CAR-T细胞作为活细胞药物,可在患者体内增殖,并可维持持续疗效长达数周甚至数月;第三具有优异的治疗效果,CAR-T细胞可通过体外改造适应多种肿瘤相关靶点和不利的肿瘤微环境,用药频次低疗效显著。
截至目前,全球已有8款CAR-T细胞产品获批上市,其中6款针对CD19靶点,2款针对BCMA靶点;8款产品中包括美国FDA批准的6款和中国NMPA批准的2款,适应症也主要集中于血液瘤。自2017年CAR-T细胞产品首次获批至今,不到5年的时间已有8款新药上市,相信在不久的将来,CAR-T细胞治疗或将势如破竹,会有更多的产品获批上市。

▲蒋华教授线上报告
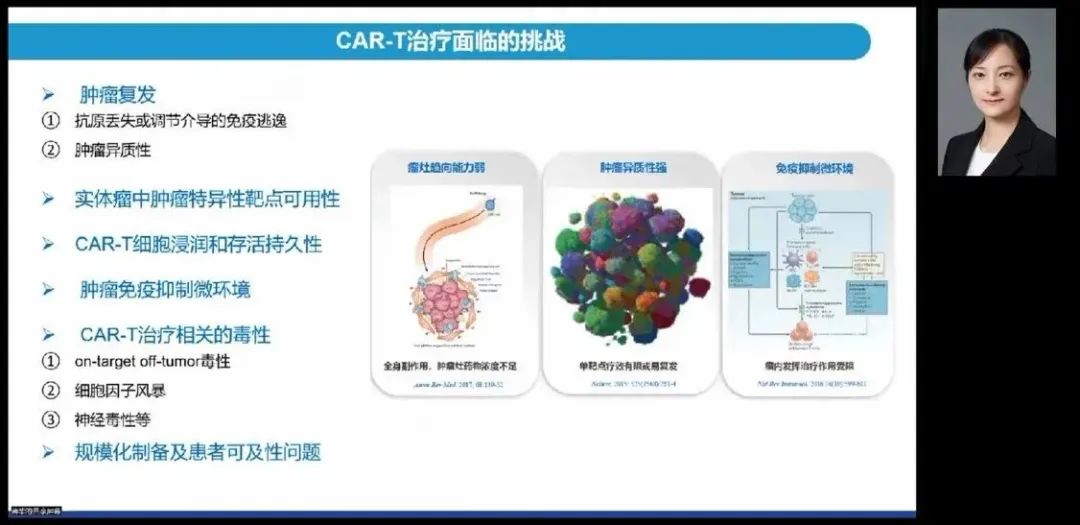
CAR-T细胞治疗虽然在肿瘤治疗中表现成功,但依然面临诸多挑战。包括肿瘤复发、实体瘤特异性靶点缺乏、CAR-T细胞浸润存活持久性、肿瘤免疫抑制微环境、CAR-T治疗相关毒性以及规模化制备和患者可及性问题等。针对这些挑战蒋教授一一做了详细介绍。首先是肿瘤复发问题,即肿瘤抗原逃逸及肿瘤异质性问题。研究发现在肿瘤复发病人中抗原阴性或低表达比例较高,蒋教授分析导致这一现象发生的原因主要有五点,第一,在药物选择性作用压力下导致抗原突变或选择性剪切从而致使CAR-T细胞无法识别;第二,肿瘤抗原表位封闭,CAR-T制备时,从患者体内提取T细胞时肿瘤细胞也被同时提取出来,导致异常转染,造成抗原表位被异位表达的CAR封闭(多见于血液肿瘤);第三,抗原表达下调导致CAR-T细胞不能有效识别;第四,与细胞谱系的转变相关,如淋巴系转化成髓系致使CAR-T细胞不能识别。第五,实体瘤中还存在基因型和表型的肿瘤异质性问题。其次,实体瘤中CAR-T细胞存活及浸润有限。与血液瘤不同,实体瘤有坚实的物理屏障,CAR-T细胞很难攻入,主要表现在致密的细胞外基质和肿瘤血管异常限制CAR-T细胞的渗透和迁移,趋化因子和黏附因子的下调致使CAR-T细胞难以定位进入肿瘤组织,另外,肿瘤微环境的缺氧、低PH值,高渗透压等因素不利于CAR-T细胞的长期存活和增殖。挑战三是实体肿瘤免疫抑制性微环境,也是面临的最大挑战之一。主要表现为免疫抑制性分子、免疫抑制细胞和细胞因子等对CAR-T细胞功能的抑制作用。挑战四为CAR-T治疗相关的毒性问题。目前共涉及7大毒性,包括细胞因子释放综合征(CRS)、神经毒性、On-Target Off-Tumor毒性、On-Target On-Tumor毒性、过敏反应、插入突变和清淋引起的相关毒性。
蒋教授分享到,针对CAR-T细胞治疗的挑战,目前研究出了多种应对策略:首先是抗原逃逸或异质性问题,研究人员提出了同时靶向多个肿瘤抗原的策略;针对实体瘤特异性靶点选择问题,尽可能选择特异性靶点,扩大治疗窗;就降低CAR-T治疗相关毒性问题,可采取依赖于小分子衔接配体的CAR-T细胞开关,还可通过药物调节CAR结构的瞬时激活结构变化,或者通过酪氨酸激酶抑制剂dasatinib抑制LCK干扰CAR-T活性,亦或通过类门控系统的多抗原调节CAR-T毒性;针对增强CAR-T细胞存活问题,目前可通过分化程度较低的T细胞亚群,或改善结构域降低T细胞过度激活,或激活DC细胞分泌免疫因子等方法来增强CAR-T细胞存活;针对CAR-T细胞的肿瘤归巢和浸润问题,可采取增加趋化因子受体表达、克服细胞外基质屏障,或通过抗血管药物治疗增强CAR-T细胞浸润,以及联合放疗或化疗增加CAR-T细胞的肿瘤浸润。就肿瘤抑制免疫微环境的挑战,目前策略是通过CAR-T细胞表达促炎细胞因子调动固有免疫,优化共刺激信号域来调节肿瘤细胞因子微环境,或通过抑制PD-1/Lag-3等免疫检查点信号分子来抵抗免疫抑制。另外,针对自体CAR-T细胞带来的制备周期长、价格昂贵、难以规模化生产等问题,目前研究人员开发的“现货”通用型CAR-T,可从“一对一”的私人定制模式发展为“一对多”的规模化生产供应,解决了现有CAR-T细胞产品“人等药”的难题,并显著降低患者治疗成本,增加患者可及性。针对这些研究策略,蒋教授团队也做了大量研究工作,并取得了很好的成绩。
最后,蒋教授表示CAR-T细胞治疗虽然遍地开花,但未来的发展之路道阻且长,仍需技术突破解决现有瓶颈问题。随着全球CAR-T细胞治疗技术的不断深入,支付体系的逐步完善,“通用型”CAR-T细胞疗法的不断发展,以及CAR-T细胞治疗临床适应症的不断扩充,未来会有越来越多的肿瘤患者获益。
▲蒋华教授线上报告
2、人工抗体组库技术与免疫治疗干预
胡适教授从肿瘤免疫治疗现状出发,介绍了肿瘤免疫编辑假说和抗肿瘤免疫应答效应等肿瘤免疫治疗相关概念,并分享了团队探索肿瘤免疫治疗相关技术的研究经验与构建人工合成免疫细胞组库的研究成果。
自PD1和CTL4肿瘤免疫疗法获得2018年诺贝尔生理学或医学奖以来,肿瘤免疫治疗手段应用广泛,但从临床结果来看,肿瘤免疫治疗整体反应率偏低,约为20%~40%,复发概率也较高,中位无病生存期约为半年。
目前,学术界对肿瘤免疫治疗的理论认识是基于肿瘤免疫编辑假说,研究者认为免疫系统首先识别并杀伤肿瘤,但在特定条件下,肿瘤细胞对免疫细胞的识别和杀伤产生了对抗,存活下来了少量的肿瘤细胞,在免疫压力下经过筛选,与免疫系统相互作用,最终造成了肿瘤细胞免疫逃逸。基于该理论,研究者设想通过人工干预、调节或者激活免疫系统,最终杀伤肿瘤细胞。
从抗肿瘤免疫应答过程来看,肿瘤组织局部存在大量的抗原递呈细胞(APC),包括树突状细胞(DC)或巨噬细胞,APC通过捕获肿瘤细胞表面抗原,并交叉呈递,最终启动肿瘤特异性抗原CD8+T细胞杀伤肿瘤。如果肿瘤直接呈现特定抗原,即可被启动的CD8+T细胞有效识别和杀伤。如果患者已经发生肿瘤复发或者转移,抗肿瘤免疫应答呈递过程则受到损伤,无法识别和杀伤肿瘤。
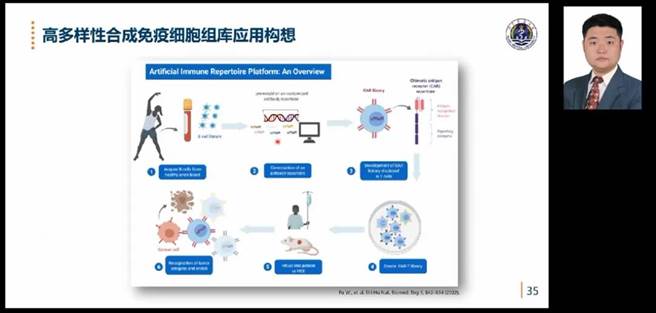
胡教授团队在抗体技术开发和免疫治疗干预做了大量工作。胡教授介绍到肿瘤分为“冷肿瘤”和“热肿瘤”,热肿瘤中存在大量CD8+,容易识别和杀伤,但冷肿瘤被识别和杀伤则比较困难。团队设想通过抗体技术干预“冷肿瘤”,能否加强抗原递呈细胞(APC)捕获肿瘤抗原,简化肿瘤免疫效应过程,以及不依赖APC抗原递呈,达到识别和杀伤“冷肿瘤”的目的。在探索抗体技术加强APC反应中,团队采取了双特异性抗体逆转巨噬细胞表型,加强cDC免疫识别,并利用工程抗体加强APC递呈时效等方法,加强APC捕获肿瘤抗原能力。在简化肿瘤免疫效应研究过程中,团队通过构建靶向递送效应T细胞小细胞外囊泡的抗体技术,实现靶向肿瘤细胞的免疫效应。研究发现在效应T细胞活化时会释放靶向性携带穿孔素和颗粒酶的小细胞外囊泡,小细胞外囊泡既具有类似效应T细胞的免疫效应功能,同时还具有肿瘤靶向性。在探索抗肿瘤不依赖APC抗原递呈的研究中,团队通过抗体技术构建工程化效应T细胞组库,证明了杀伤肿瘤可不依赖于APC抗原呈递。在这一研究过程中团队受到了启发,产生了构建人工合成抗肿瘤免疫的设想。基于此构想,团队设计了研究路线,对免疫细胞进行基因编辑,形成了一种工程化的免疫细胞,后将特定抗体编辑到CAR抗体上转染细胞,得到多克隆的嵌合抗原受体的细胞组库,这样细胞组库即获得了多样性的嵌合抗原受体合集。经过微小规模和大规模的组库验证,最终合成了可识别超106种未知抗原的多样化的免疫细胞组库,胡教授表示,当细胞识别肿瘤组织中未知抗原后,该工程化细胞组库可在多个细胞系肿瘤体内模型中响应富集,并杀伤肿瘤细胞。另外,研究发现合成的细胞组库具有维持免疫力的特性,当肿瘤组织抗原由于免疫压力造成变化时,细胞组库还可以进化产生全新的效应细胞,因此该合成细胞组库可以有效解决恶性肿瘤异质性、进化和逃逸问题。该成果显示了多样性嵌合抗原受体的合成免疫细胞组库可作为一种有效的癌症免疫疗法,并于2022年发表在Nature Biomedical Engineering期刊上。
在肿瘤免疫研究中,研究者对抗体的特异性和免疫效应研究较多,但对抗体多样性研究仅作为抗体特异性研究的基础,胡教授表示抗体的多样性研究对肿瘤免疫治疗具有重要意义,可作为肿瘤治疗的突破口深度研究。
▲胡适教授线上报告
Science Café 沙龙
Science café 沙龙是由上海市药物研发协同创新中心与浦东国际人才发展中心共同举办,集信息交流、头脑激荡、创意融合的跨界协调合作的平台。一期一会,一杯咖啡,汇聚集体智慧,多角度探讨生物医药的创新前沿话题。
若您有感兴趣的生物医药创新前沿话题或有合作意向,欢迎通过以下方式与我们取得联系,期待与您携手共进。
联系人:凌女士
联系电话:58336301、15000788873